| |
|
|
|
|
|
|
|
|
 |
多発性骨髄腫とは
|
|
|
|
|
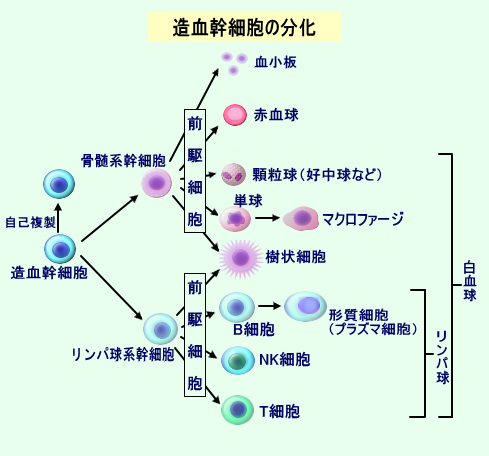
骨髄で造血幹細胞から作られるリンパ系前駆細胞がつくられますが,この細胞は最後にはB細胞やT細胞になり,B細胞はさらに形質細胞とよばれるものに分化します。
| すなわち,B細胞の最も成熟したものが形質細胞であり,プラズマ細胞とも呼ばれています。 |
スポンサードリンク |
| |
|
 |
|
体内に侵入した病原菌などの異物を排除する抗体をつくるのが,この形質細胞であり,多発性骨髄腫はこの形質細胞が,がん化したものです。
多発性骨髄腫になると,がん化した形質細胞(骨髄腫細胞)が全身の骨髄で増殖を続け,通常の10倍以上に増加してしまいます。 |
形質細胞は免疫グロブリンという抗体タンパクを作り,体内に侵入した細菌やウィルスを攻撃します。
ところが,がん化した形質細胞で作られた免疫グロブリンは抗体として機能せず,細菌やウィルスを攻撃するはたらきはほとんどありません。
このような異常な免疫グロブリンはMタンパクと呼ばれていますが,このMタンパクは体に多くの障害を引き起こすことがわかっています。
たとえば,血流を悪化させ,腎臓の尿細管をつまらせ,心臓や消化管の神経に取りつき,その機能を低下させたりします。
このように,多くの症状が同時に多発することから,このがんは多発性骨髄腫と呼ばれるようになりました。
このような症状の中でも最も深刻ともいえる障害が,この骨髄腫細胞により,体の骨が破壊されていくことです。
この骨髄腫細胞は古い骨を破壊する作用のある破骨細胞を刺激し,骨を際限なく破壊してしていくようになります。 この結果,骨の痛みや骨折などが生じるようになります。
また,一方で,正常な免疫グロブリンは減少するため,免疫機能が低下して,肺炎などの感染症にかかりやすくなったりします。さらに,正常な血液細胞が産生できず,貧血や出血が起こりやすくなったりします。
これまで,多発性骨髄腫の治癒は困難であるといわれ,平均生存期間は3~4年で,10年以上の生存率は約3~5%といわれていました。
しかし,最近になり,サリドマイド,ボルテゾミブ,レナリミドなどの抗がん剤の新薬が承認され,生存率は大幅に向上しています。
|
|
 |
多発性骨髄腫の進行度と治療方針
|
|
|
多発性骨髄腫の病期は一般的にはDurie and Saimon病期分類が使用されます。(下図参照)
この病期分類では貧血の状態を示すヘモグロビン値,血清カルシウム値,エックス線検査による骨病変の程度,Mタンパク量の4つの項目から成り立っています。
多発性骨髄腫の進行速度は遅いため,病期Ⅰの段階では通常,経過観察のみで治療は行いません。
治療を開始するのは病期Ⅱ期になってからです。
 多発性骨髄腫の病期と標準治療 (Durie and Saimon病期分類による) 多発性骨髄腫の病期と標準治療 (Durie and Saimon病期分類による)
| 病期 |
検査結果 |
標準治療法 |
| Ⅰ期 |
次の三つの基準を満たす
ヘモグロビン:>10g/dℓ
血清カルシウム値:正常
骨エックス線像:正常または孤立性形質細胞腫
Mタンパク量
IgG:く5g/dℓ
IgA:<3g/dℓ
尿ペンス・ジョーンズタンパク:く4g/dℓ
(免疫グロブリンの一種)
|
経過観察 |
| Ⅱ期 |
病期Ⅰでも病期Ⅲでもない |
薬物療法 |
| Ⅲ期 |
次の一つ以上の基準を満たす
ヘモグロビン:く8.5g/dℓ
血清カルシウム値:>12mg/dℓ
骨エックス線像:広範な骨融解像
Mタンパク量
IgG:>7g/dℓ
IgA:>5g/dℓ
尿ペンス・ジョーンズタンパク>12g /日
(免疫グロブリンの一種) |
薬物療法
または
造血幹細胞移植 |
| 亜分類 |
A:腎機能が正常に近い
(血清クレアチニン値<2.0mg/dℓ
B:腎機能異常
(血清クレアチニン値≧2.0Omg/dℓ |
|
|
|
 |
多発性骨髄腫の抗がん剤治療
|
|
|
多発性骨髄腫は全身に広がっている病気のため,抗がん剤治療が中心です。 ただし,1ヶ所だけに腫瘍をつくる形質細胞腫や,骨折の危険性がある病変や,痛みの緩和のため,放射線療法や手術を行うこともあります。
多発性骨髄腫ではⅡ期以降に治療をはじめますが,治療方針は,65歳で変わります。
65歳以下の患者では,重い合併症や臓器障害がなければ,初回治療は大量化学療法と自家造血幹細胞移植を組みあわせた治療を行います。
また,65歳以下や,65歳未満でも移植を希望しない場合は多剤併用の化学療法を行います。
この理由は高齢になると,骨髄移植に必要な前処置の負担が大きくなり,特に,他人の造血幹細胞移植をおこなった場合,合併症が増加してしまうからです。
65歳以上では,従来型の抗がん剤と新しい分子標的薬を中心とした治療を行います。
現在では,多発性骨髄腫の治療において,分子標的薬のボルテソミブ(ベルケイド)やサリドマイド(サレド),レナリドミド(レブラミド)が登場することにより,QOLを維持しながら,生存期間も延長できるようになりました。
 |
造血幹細胞移植+大量化学療法 (65歳未満で造血幹細胞移植が前提の場合) |
多発性骨髄腫などの血液腫瘍は,抗がん剤治療の効果が高く,治癒も期待できます。
治療効果を高めるため,抗がん剤を大量投与した場合には,骨髄のダメージが大きく,白血球をはじめ,赤血球や血小板が減少し,回復できないこともあります。
そこで,大量の投与によって,がん細胞を強く攻撃するとともに,骨髄機能・免疫機能を抑制し(移植前処置),その後,造血幹細胞を点滴で投入し,正常な血液が造られるようにするという方法おこなわれるようになりました。これを造血幹細胞移植といいます。
まず,65歳未満で移植が前提の場合や,65歳以上でも腫瘍量が多くて急速に進行していると判断されるときは,ボルテゾミブとデキサメタソンを併用する「VD療法」や,VD療法にシクロホスファミドを併用する「VCD療法」がおこなわれます。
次に造血幹細胞移植の前処置として,シクロホスファミドやエトポシド,メルファランをを大量に投与します。
副作用としては吐き気・嘔吐・下痢・口内炎などがあり,通常約2週間続きます。脱毛も見られます。
その他,心臓,肝臓,腎臓などへの障害や膀胱炎が起こることもあり,その予防のために治療中は大量の輸血を行います
移植自体は輸血とほとんど同じ方法で,採取した造血幹細胞を含んだ骨髄血あるいは血液を,点滴で投与します。 輸血された造血幹細胞は骨髄にたどり着き,そこで働き始めます。
白血球が少なくなると感染症を起し易くなります。そのため無菌室に入ります。
特に血小板の減少は,出血の危険を伴うため,血小板の輸血を行います。また貧血には赤血球輸血を行います。 移植した造血幹細胞が骨髄に定着し,造血機能を回復するまで平均3週間かかります。
造血幹細胞移植には,「自家移植」と「同種移植」があります。自家移植とは患者自身の造血幹細胞を移植する方法です。
患者自身の細胞なので拒絶反応は起こりませんが,採取した造血幹細胞にがん細胞が含まれている可能性があり,治癒率はやや下がります。
一方の同種移植とは,他人の造血幹細胞を移植する方法です。
自家移植よりも根治率は高いものの,移植した細胞が患者自身の細胞を攻撃する「移植片対宿主病(GVHD)」と呼ばれる拒絶反応が起こることがあるため,免疫抑制薬などが使われます。
また,移植後の地固め療法として,ボルテゾミブ,サリドマイド,デキサメタゾンを併用する「VTD療法」や,維持療法として,レナリドミドやボルテゾミブが有効とされています。
 |
造血幹細胞移植が不能な場合の抗がん剤治療(MP療法・VMP療法)
|
65歳以上や,65歳未満でも造血幹細胞移植ができない場合,現在,標準治療となっている治療法が,アルキル化剤のメルファランとステロイド薬のプレドニゾロン(MP療法)に,ボルテゾミブを併用する「VMP療法」とよばれる抗がん剤治療です。
国内外の臨床試験で,VMP療法はMP療法と比べて,奏効率が倍以上に改善し,生存期間が延長することが明らかになっています。
また高齢の患者には、年齢や全身状態に応じて,ボルテソミブやメルファラン,プレドニゾロンの用量調整も行います。
再発した場合の2次治療では,初回時にVMP療法で奏効が得られた場合にはボルテソミブ併用療法の再治療がおこなわれ,効果が得られなかった場合は「レナリドミド+デキサメタゾンン療法」がおこなわれます。
|
|
|
|
|
|
| |
| |
|